
В США на стадии разработки находится 452 кандидата в препараты для лечения редких заболеваний
18 Ноября 2013
Согласно отчету Ассоциации исследователей и производителей фармацевтической продукции США (Pharmaceutical Research and Manufacturers of America), в биофармацевтических компаниях США на стадии разработки находится 452 кандидата в препараты для лечения редких (орфанных) заболеваний. Так, проводятся клинические исследования упомянутых лекарственных средств или заявки на их одобрение находятся на рассмотрении в Управлении по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA). Из них 105 предназначены для терапии онкологических заболеваний, 85 — наследственной патологии, 65 — лейкемии, 32 — неврологических расстройств, 28 — инфекционных и 20 — респираторных заболеваний (рисунок). Среди других разработок — кандидаты в препараты для лечения аутоиммунных заболеваний, нарушений со стороны органа зрения, заболеваний кожи, крови, сердечно-сосудистой системы, нарушения пищеварения, роста.
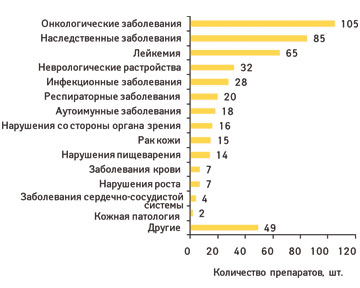
Орфанные препараты, находящиеся на стадии разработки в США
По материалам www.phrma.org
PrintНаши новости
Медиа-центр
-
В ЕАЭС вступило в силу положение о взаимном признании ученых степеней
07 Мая 2024
-
Главой офиса ВОЗ в России назначен Батыр Бердыклычев
07 Мая 2024
-
В России может появиться Федеральный центр качества технических средств реабилитацииэ
06 Мая 2024
-
ФМБА: санкции дали новый импульс к развитию разработок и самодостаточности РФ
06 Мая 2024